Investigación Biomédica en CCSS
La Caja Costarricense de Seguro Social (CCSS) cuenta con una red de Comités Éticos Científicos para regular la investigación biomédica en sus centros asistenciales, organizada de acuerdo con la Red de Servicios de Salud.
Toda investigación biomédica que se pretenda realizar en los centros asistenciales de la CCSS, que utilice algún insumo institucional, que requiera la participación de pacientes, o la utilización de sus datos, debe ser aprobada por un Comité Ético Científico de la CCSS, acreditado por el Consejo Nacional de Investigación en Salud (CONIS). (Artículo 3º y 12º Reglamento de Investigación Biomédica de la CCSS publicado el pasado 10 de marzo 2021, en el Diario Oficial La Gaceta)
Según la estructura organizativa institucional, es el CEC-CENTRAL-CCSS quien analiza los protocolos que cumplan con al menos uno de los siguientes criterios:
- Multicéntricos.
- Intervencionales.
- Genéticos.
- Con patrocinio externo.
Mientras que los CEC-locales podrán analizar protocolos observacionales y unicéntricos.
Recepción de solicitudes para revisión de protocolos de investigación biomédica
El Área de Bioética del CENDEISSS comunica que la recepción de solicitudes de revisión de protocolos de investigación biomédica por el Comité Ético Científico Central de la CCSS (CEC-CENTRAL-CCSS) se hará por medio del correo electrónico bioetica@ccss.sa.cr, los días lunes, martes y miércoles.
También se podrá hacer entrega de la documentación en formato impreso en la oficina de esta Área, situada en el piso 3 del CENDEISSS, en el siguiente horario:
- Lunes, de 1:00 pm a 2:45 p.m.
- Martes, de 8:00 am a 2:30 p.m.
- Miércoles, de 8:00 am a 2:30 p.m.
**No se recibirán solicitudes de revisión de protocolos de investigación biomédica los días jueves y viernes**
Los documentos de sometimiento remitidos por medio electrónico deberán ser firmados en su totalidad con firma digital; no se aceptan firmas híbridas (combinaciones de firmas digitales con físicas).
Adicionalmente, los siguientes son los CEC locales de la Institución acreditados por el CONIS:
Oficios de interés
CENDEISSS-AB-0096-2022 Investigación Biomédica en la CCSS.
CENDEISSS-AB-0058-2023 Recordatorio Investigacion Biomédica.
CENDEISSS-AB-0174-2023 RECORDATORIO RESPONSABILIDADES EN MATERIA DE INVESTIGAC.
CENDEISSS-AB-0328-2023 Recordatorio Obligaciones para Investigadores.
Guía Interna Configuración Firma Digital.
Documentos para presentar investigaciones biomédicas observacionales
Las investigaciones biomédicas observacionales serán analizadas por el CEC local o el CEC-CENTRAL según corresponda, y de acuerdo con la Red de Servicios de Salud.
Para solicitar el sometimiento, aprobación y autorización al CEC-CENTRAL se deben presentar los siguientes formularios en la fecha que corresponda (Ver calendario sesiones CEC).
Para solicitar el sometimiento en los CEC locales deben consultarles directamente los horarios y calendarios para su recepción.
Documentos para presentación de investigaciones observacionales
Documentos para presentar investigaciones biomédicas intervencionales
- Para el caso de investigaciones biomédicas experimentales o intervencionales, serán analizadas por Comité Ético Científico Central (CEC-CENTRAL-CCSS), se deben presentar los formularios en la fecha que corresponda (Ver calendario sesiones CEC).
Documentos para presentación de investigaciones intervencionales
Tarifas del Comité Ético Científico Central de la CCSS
De acuerdo con el Modelo Tarifario I semestre 2024, las tarifas a cancelar a la CCSS por concepto de revisión, renovación y enmienda de protocolos de investigación biomédica con patrocinio externo por parte del CEC-Central de la Institución, son las siguientes:
| Descripción | Modelo Tarifario* |
| Solicitud enmienda | ₡50 246 |
| Solicitud primera vez | ₡1 402 001 |
| Solicitud renovación anual | ₡821 910 |
*Incluye el 25% de gastos administrativos, según Modelo Tarifario del Seguro de Salud vigente a partir del 01 de enero del 2024.
El proceso de solicitud de pago es el siguiente:
- El investigador antes de presentar a la Secretaría Técnica la documentación para revisión por parte del CEC, debe solicitar al Área de Bioética, mediante el correo electrónico bioetica@ccss.sa.cr, el Formulario para Pago de Investigaciones Biomédicas, en el cual se establecerá el medio de pago.
- Los pagos por este concepto se pueden realizar únicamente mediante Comprobante SICO o transferencia bancaria.
- El Área de Bioética remite por correo electrónico al investigador el Formulario para Pago de Investigaciones Biomédicas para el llenado de la información e indicación del medio de pago a utilizar.
- Una vez que el investigador o patrocinador remita el Formulario para Pago de Investigaciones Biomédicas, el Área de Bioética verificará la información y gestionará el número de SICO en caso de pagos en efectivo, para que pueda realizar el pago en las oficinas centrales de la CCSS o en cualquier sucursal. Este debe realizarse el mismo día que se genera el número de SICO.
- Los pagos mediante depósito bancario se podrán realizar en moneda extranjera por medio de las cuentas establecidas por la CCSS y disponibles en el Formulario para Pago de Investigaciones Biomédicas. Para las cuentas en moneda extranjera se debe convertir el depósito a colones al tipo de cambio de compra indicado por el Banco Central, del día que ingresó el dinero a la Institución.
- Seguidamente, corresponde al investigador presentar a la Secretaría Técnica del CEC-Central, la documentación completa de su solicitud (revisión, renovación o enmienda, según corresponda), junto con el comprobante de pago y el Formulario para Pago de Investigaciones Biomédicas remitido con firma de la persona responsable del Área de Bioética.
- Las investigaciones con patrocinio de instituciones públicas no pagan los aranceles indicados. En la declaración de fuentes de financiamiento el investigador debe indicar que los recursos son de la institución pública y aportar una carta oficial en la que se haga constar el origen de los fondos. Consultas a los teléfonos 2519-3081, 2519-3080, 2519-3051, 2519-3046.
Cronograma para la presentación de los informes trimestrales de avance de investigaciones biomédicas
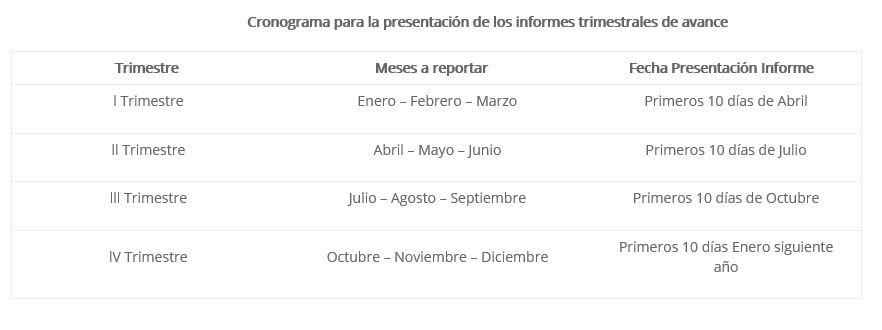
Presentación de los informes anuales de investigaciones biomédicas
FECHA PRESENTACIÓN INFORME
Una vez cumplido un año de la aprobación, tendrá en un plazo no mayor a 30 días naturales para la presentación.
A manera de ejemplo;
1.- Fecha de aprobación 01 de mayo 2020.
2.- Cumple un año el 30 de abril 2021.
3.- El informe se debe presentar a más tardar el 31 de mayo 2021.